为探究细胞在生命体中完整而真实的“职业生涯”,中国科学院分子细胞科学卓越创新中心周斌研究组开发了一种独特的遗传操作技术,它可以给在特定环境中待过的细胞带上标记,好像找到“同桌的你”,并不断追踪它迁移到别的器官,进入不同微环境的过程。
这种名为“邻近细胞遗传学技术”的新工具,为研究细胞在生命体中错综复杂的“社会行为”开拓了一个全新的维度。12月2日凌晨,相关论文发表在国际著名学术期刊《科学》上。
“在人体内,细胞经常会‘搬家’。”周斌团队在研究中发现,如果将人体看作一个“生命社会”,细胞就像社会中的公民,其中有不少细胞会在不同的器官之间迁徙,并随着新的‘邻居’和微环境变成不同的样子。“就好像我国古代的孟母三迁,每换一个环境,孩子就会受到不同的影响。”
早在十多年前,“追踪细胞的迁移足迹,找到环境带给它的改变”就成了周斌研究员日思夜想要解决的科学问题。
怎样让环境给细胞打上特定的标记?“对于心脏来说,心肌细胞是独一无二的代表。只要与心肌细胞有接触,就代表这个细胞曾在心脏里待过。”于是,周斌想出一个办法:用合成生物学的方法,制造出一对人工“对牌”,再结合传统的遗传学操作技术,给心肌细胞与被追踪细胞分别带上一半人工“对牌”,两者只要在体内相遇,人工“对牌”就会配对并点亮被跟踪细胞的荧光标记——不管在下一站被追踪细胞变成了什么样,科学家都能通过荧光标记精准认出曾与心肌细胞“同桌”的它。
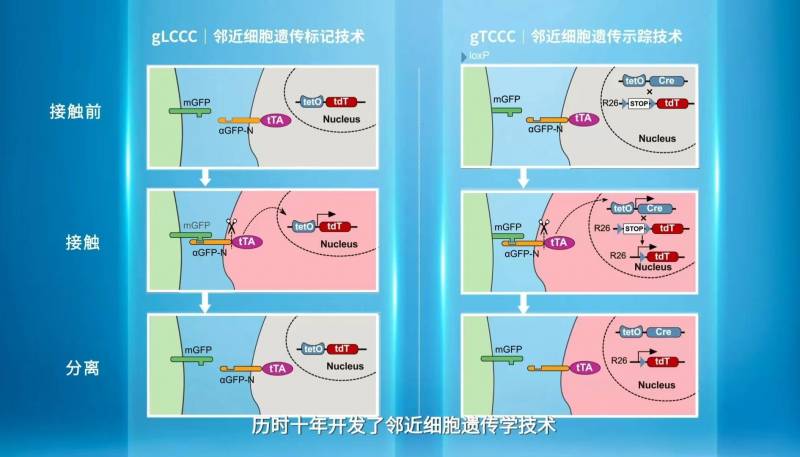
“这样,我们就能非常方便地将它取出,并通过测序,找出体内微环境对它的改变。”周斌介绍,利用这种方法,他们发现,心脏中的内皮细胞在早期胚胎发育过程中会迁移到肝脏,并在肝脏组织的微环境影响下,转变成为肝脏特有的肝血窦内皮细胞。“由此可见,细胞间的互作及所处环境对细胞命运和功能转变至关重要。”
在这项研究中,研究人员还利用邻近细胞遗传学技术,直观展现了不同阶段肿瘤细胞和血管内皮细胞间的动态相互作用,并通过长时程追踪发现肿瘤血管内皮细胞会迁移到肿瘤外包膜。这部分肿瘤血管内皮细胞仍然具有典型的转移和浸润、促血管生成以及炎症反应等特征,说明细胞进入新环境后,最初环境赋予细胞的影响可能仍然存在。
历经近十年,周斌与论文两位靠前作者——周斌研究组的博士后张少华和副研究员赵欢博士,失败过无数次。“我们前后培育了50多个小鼠品系,”周斌希望,今后可以不断优化,让更多实验室能用上这种全新的技术,打开观察生命活动的全新维度。
这一新技术突破了传统示踪技术的局限,实现了邻近细胞的遗传操作,为发育生物学、肿瘤学、干细胞生物学和免疫学等众多领域研究提供了新的研究思路和强大技术支撑,具有广阔应用前景。
作者:许琦敏
图片:受访者提供






